AABB认证咨询-AABB《细胞与基因治疗药学标准》10 月 1 日生效 填补专业药房管理空白
2025 年 8 月,全球血液与生物治疗领域权威组织 AABB 正式宣布,《细胞与基因治疗药学标准》(第一版)将于 10 月 1 日起正式生效。这一标准的出台填补了细胞与基因治疗(CGT)产品在专业药房管理领域的标准空白,为快速发展的先进疗法提供了关键的质量保障框架。作为目前全球唯一为经营细胞与基因治疗产品的专业药房制定标准的组织,AABB 的这一举措将显著提升 CGT 产品从储存到分发全链条的安全性与有效性。
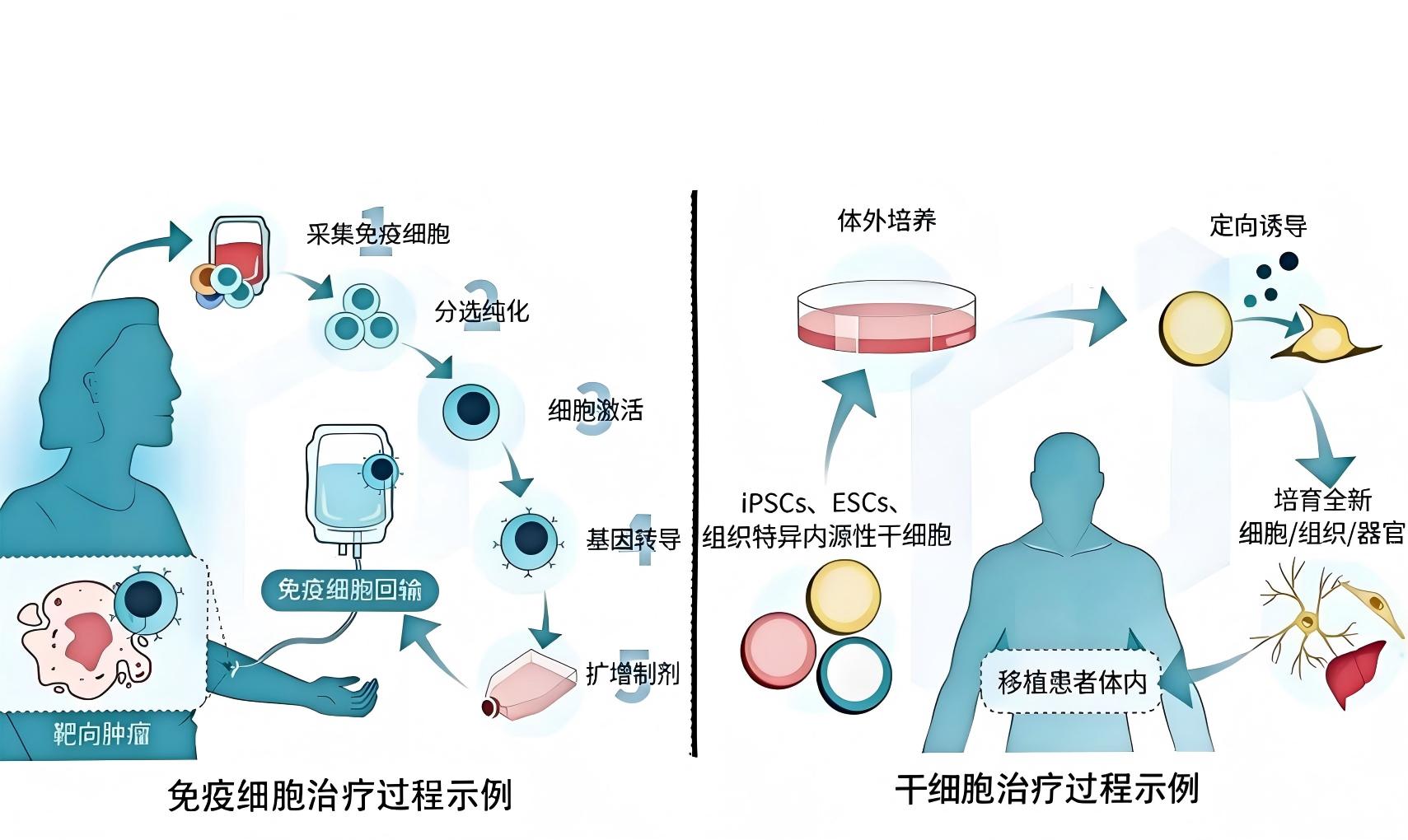
近年来,细胞与基因治疗领域呈现爆发式增长态势。数据显示,2023 至 2027 年全球细胞治疗市场复合年增长率高达 57.06%,预计 2031 年全球细胞和基因疗法药品市场规模将达到 520.8 亿美元。我国在该领域的发展同样迅猛,2023 年度全球细胞治疗临床研究中,我国占比约 30%,超过 800 项临床研究正在开展,跻身全球第一梯队。随着 CAR-T 细胞疗法等创新疗法的快速获批,仅我国就已有 9 项新药上市申请获得批准,专业药房在这些高价值、高复杂性治疗产品的分配管理中扮演着日益关键的角色。
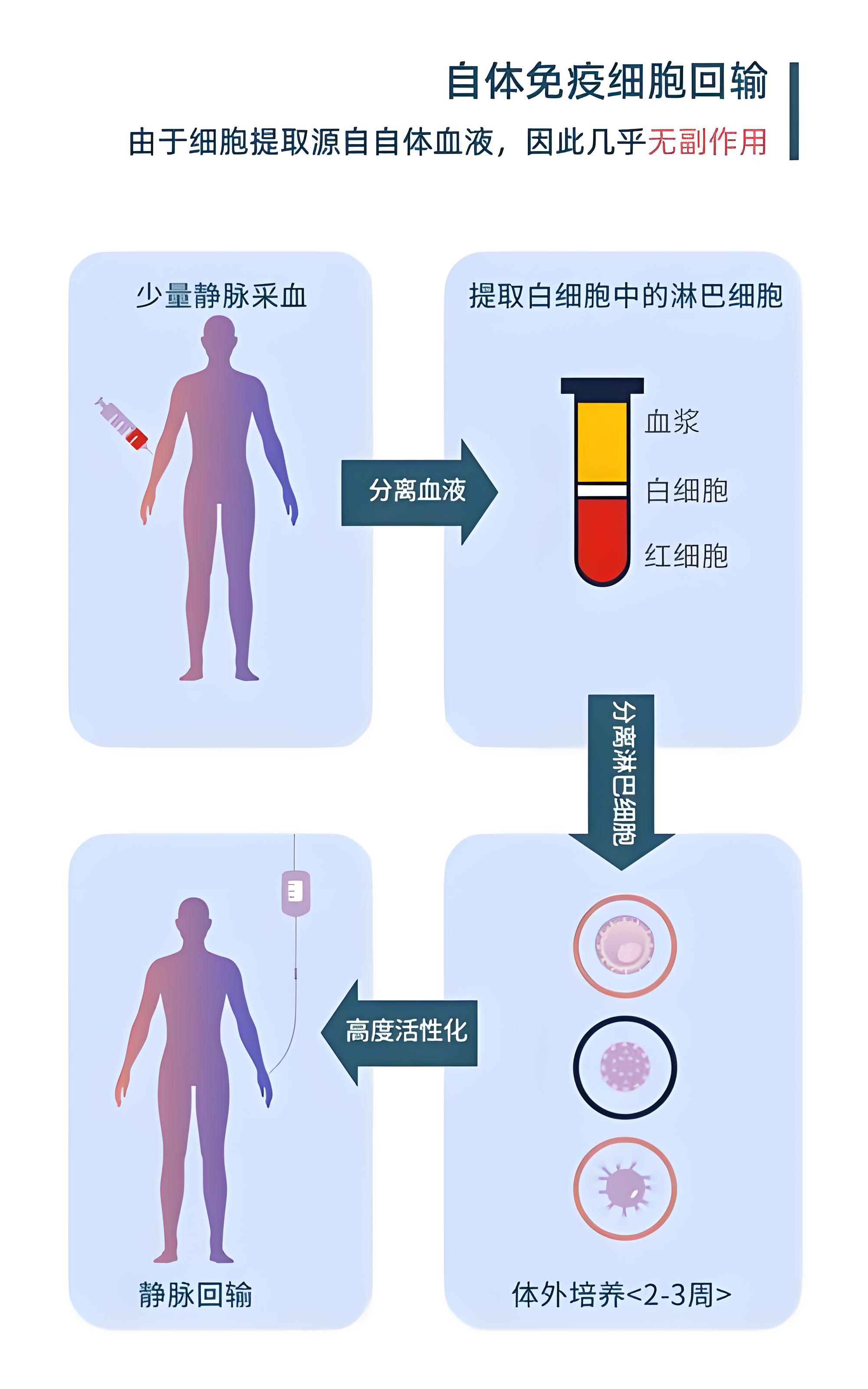
然而,现有药房质量标准体系未能跟上技术革新的步伐。AABB 在调研中发现,传统药房认证标准未考虑细胞与基因治疗产品的特殊性,缺乏针对其特殊储存、处理和分发要求的专项规定。这类先进疗法对保存条件有着极其严苛的要求,通常需要在 - 130°C 以下的超低温环境中储存,以确保细胞活力和治疗效力,运输过程中还需实时温度监控和应急方案。海南博鳌乐城国际医疗旅游先行区近期公布的第三批 CGT 新技术项目显示,单次细胞治疗费用从 1.6 万元到 14 万元不等,如此高昂的治疗成本一旦因管理不当导致失效,不仅造成经济损失,更直接威胁患者的治疗机会。
作为拥有 78 年历史的国际权威标准制定机构,AABB 凭借其在血液和细胞治疗领域 25 年以上的标准制定经验,组建了由跨领域专家构成的细胞与基因治疗药学标准委员会。该委员会汇集了美国红十字会、CVS 健康、斯坦福医院、FDA 治疗产品办公室等 14 家机构的专业代表,涵盖了从产品研发、生产到临床应用的全产业链环节,确保标准的科学性和实用性。AABB 首席科学官在声明中表示:"这一标准的制定过程充分体现了行业协作精神,我们结合了前沿科研成果、临床实践经验和监管要求,打造出既严谨又具操作性的管理框架。"
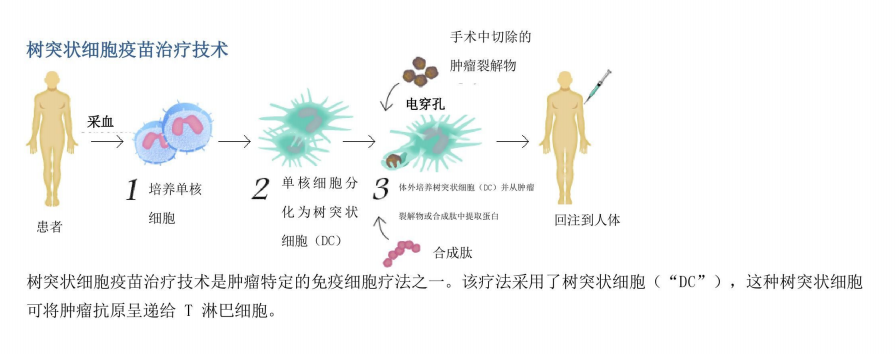
《细胞与基因治疗药学标准》(第一版)聚焦专业药房在 CGT 产品接收、储存、处理和分发环节的质量体系建设,明确了人员资质、设施要求、操作规范和质量控制等关键要素。与传统标准不同,该标准充分考虑了活细胞产品的特殊性,对超低温储存设备的校准频率、温度偏差的应急处理、人员培训的核心内容等都做出了详细规定。配套出版的《细胞与基因治疗药学标准指南》采用创新编排方式,在标准条款后直接附上实施指导内容,便于用户同步查阅要求与操作建议。
值得注意的是,标准制定采用了优先级策略,优先为需要额外背景说明的条款提供指导。AABB 解释称,这一做法旨在确保资源集中用于最关键的实施难点,未提供指导的条款将根据实施反馈在未来更新中补充完善。这种动态完善机制使标准既能及时应对当前需求,又为未来技术发展预留了调整空间。

此次发布的合订套装包括标准文本(91 页,ISBN 978-1-56395-527-3)和配套指南(65 页),于 2025 年正式出版发售。标准有效期为两年,AABB 计划在实施过程中收集行业反馈,结合技术进步和监管变化进行修订更新,确保标准的时效性和先进性。
业内专家普遍认为,该标准的出台将对细胞与基因治疗行业产生深远影响。斯坦福医院药房主任指出:"专业药房长期面临 CGT 产品管理无据可依的困境,AABB 标准的发布填补了这一关键缺口,有助于提升整个行业的质量管理水平。" 更重要的是,标准的统一将降低跨机构合作的沟通成本,促进治疗技术的规范推广,使更多患者受益于创新疗法。
 关键字
关键字
 联系方式
联系方式

 {{ articleInfo.phone }}
{{ articleInfo.phone }}
 {{ articleInfo.email }}
{{ articleInfo.email }}
 深圳市龙岗区平湖街道平安大道1号华耀城12栋605
深圳市龙岗区平湖街道平安大道1号华耀城12栋605













 18576401396
18576401396